作者:阿帕克生物
前 言
免疫PET的应用需要在温和的条件下对抗体载体进行简单、快速和特异性的放射性核素(示踪剂)标记。最佳的免疫PET成像归因于高度特异性的肿瘤摄取和低背景保留。为此,示踪剂必须尽可能快地饱和其目标,而未结合的示踪剂将迅速从血液循环中清除出来。一般来说,免疫PET探针的成功开发高度依赖于肿瘤靶向载体、放射性核素、双功能螯合剂和偶联策略的选择。
· 放射性核素的标记策略
基于Lys的随机偶联是抗体化学修饰最常用的方法,其次是基于Cys的偶联。虽然许多临床级抗体是通过Lys进行放射性标记,但是这种随机性的标记也可能会出现在不适合的位点(如CDR区),标记这些位点后形成的空间位阻可能会损害放射性标记抗体最终的免疫反应和相关分布。因此,人们不断致力于开发位点特异性偶联策略,以生产用于高质量成像、定义明确的放射性示踪剂。
常见的偶联策略如下:
1. 传统的定点标记
通过标准蛋白工程技术和重组表达系统,可以使蛋白质或抗体与短肽标签进行融合表达,达到特异性的位点修饰的目的。一般情况下,尝试在mAbs或sdAbs的C端引入标签,以避免其干扰与抗原的结合。Cys工程是抗体载体位点特异性放射性标记最常用的方法(图1)。经典Cys修饰是通过马来酰亚胺偶联,这种偶联方式是可逆的,并且可能导致马来酰亚胺支架在血浆中的断裂与释放。新一代的马来酰亚胺类试剂(碳基丙烯酸试剂),能够克服这一缺陷,形成稳健的生物共轭键,为实现不可逆Cys生物偶联的新策略提供参考。
由于生物医学领域的不断进步,针对蛋白质进行位点特异性修饰的技术正在呈指数级发展。未来的研究可能会利用这些新兴技术合成新的免疫PET制剂。
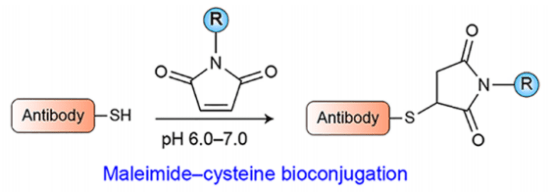
图1.马来酰亚胺−半胱氨酸反应是抗体载体位点特异性放射性标记最常用的策略之一,R=螯合剂.
2. 点击化学介导的放射性标记
点击化学(Click chemistry),又译为“链接化学”、“速配接合组合式化学”,是由化学家巴里·夏普莱斯(K B Sharpless)在2001年引入的一个合成概念,主旨是通过小单元的拼接,来快速可靠地完成形形色色分子的化学合成。点击化学介导的偶联已被越来越多地应用于开发新的分子成像探针,且通过点击化学反应进行放射性标记是双向的。在各种点击化学反应中,由Cu(I)催化的叠氮化物和炔烃之间的1,3 -偶极环加成反应(CuAAC)经常被用于开发放射性药物。通过CuAAC反应制备的F标记小分子探针在临床环境中被广泛应用与评估。但在开发具有放射性金属核素的免疫PET探针时,不得不放弃使用Cu(I)催化剂,一种常见的替代方法,叠氮化物−炔环加成(SPAAC)反应(图2),其不需要催化剂便可进行的标记方式在放射性金属核素中得以应用。
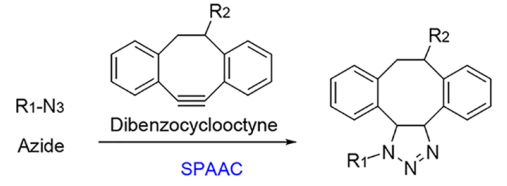
图2. 菌株促进叠氮化物−炔环加成(SPAAC)反应。R1=抗体,R2=螯合剂.
然而,环辛基前体在SPAAC系统中合成的复杂性和疏水性可能会限制其广泛的应用。反式环辛烯(TCO)和缺电子四嗪(Tz)之间的反电子需求 Diels−Alder(IEDDA)反应是生物正交化学在反应性和应用可能性等领域向前迈出的一大步(图3)。因此,这种化学方法已经被广泛应用于开发分子成像探针。
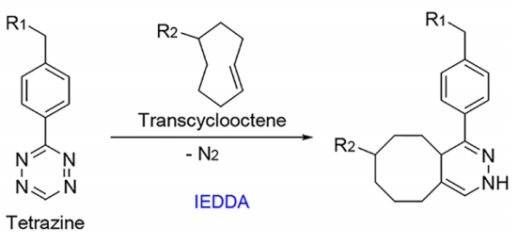
图3. 逆电子需求Diels−Alder(IEDDA)环加成反应。R1=螯合剂,R2=抗体。
3. 酶介导的放射性标记
3.1 分选酶A(SrtA)
以酶介导的方法非常适合于实现抗体载体的位点特异性标记。其中最突出的是利用分选酶A(SrtA),一种主要来源于革兰氏阳性金黄色葡萄球菌的酶。通常,SrtA识别含有C端LPXTG基序的底物(其中X代表除脯氨酸外的任何氨基酸),并切割苏氨酸(Thr)和甘氨酸(Gly)之间的肽,导致底物下游部分(例, his标签)的丢失,并与含有N端甘氨酸残基的亲核底物形成新的肽键。SrtA是一种成熟的酶,负责将含有LPXTG的蛋白质锚定在各种革兰氏阳性细菌正在生长的细胞壁和菌毛上,同时重组SrtA近年来已发展成为一种有价值的蛋白质工程工具。通过使用SrtA的转化,很容易将功能部分(如螯合剂和染料)安装到抗体的N-端或C-端(图4)。
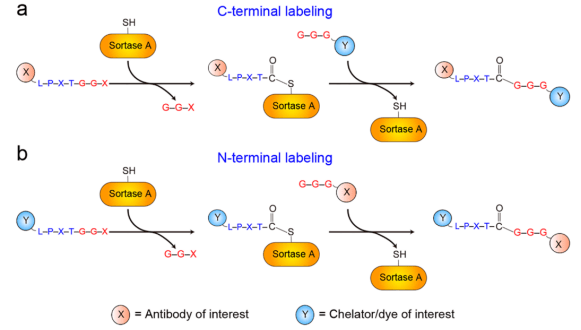
图4. 分选酶催化的抗体部分的位点特异性标记,a=C端/b=N端.
SrtA的使用促进了以18F进行的VHH的位点特异性放射性标记。同时一种独特的两步模块化系统(图5)也可以用来偶联免疫PET探针。在该体系中,使用SrtA将应变的环辛基官能团加入到感兴趣的目标载体中,然后在点击化学处理之间进行叠氮化物−炔烃环加成反应。
图5. Sortase A(Srt A)介导螯合剂与scFvanti-LIBS-LPETGG-FLAG的偶联,然后释放和分离FLAG亲和标签,并对产物进行64Cu标记.
随着SrtA催化活性的进一步提高和Ca2+非依赖型的SrtA突变体的开发,SrtA将作为开发更复杂的免疫PET探针的多功能平台。
3.2 Butelase1(蝶豆粘酶)
Butelase1是来源于东南亚药用植物蝶豆花(clitoriaternatea)的豆荚中一种特异性连接酶,它能高效催化羧基末端为Asx(sp/sn)-His-Val的线性多肽。Butelase1将线性多肽羧基末端的His-Val二肽切割掉后与氨基端相连,形成环状结构。环化后的多肽其抵抗蛋白酶水解、高温变性及耐受极端化学条件的能力都明显提高,同时其半衰期和原有的生物活性也有所提升。
尽管它是最快的肽连接酶,但它的生物学应用却十分有限,因为它目前还不能使用重组技术生产。理论上,Butelase1和SrtA的结合可有助于蛋白质在两个不同位点的标记。Harmand等人最近的一项工作证实了这一点,该研究报道SrtA和butelase 1的结合可以轻松制备C-C融合蛋白,并可同时用两种染料对IgG1分子进行双标记。`组合Butelase1与其他转肽酶在未来是可能的。基于此设想,近期发明出一种将聚糖工程和点击化学结合的化学酶策略。此策略的联合使用允许分子位点特异性地附着在重链聚糖上。
该方法包括以下步骤:
(1)使用β-1,4-半乳糖苷酶去除抗体重链甲烯域上的半乳糖残基
(2)使用β-半乳糖基转移酶突变体到Gal-T(Y289L)将叠氮化物修饰的单糖附着到重链聚糖上
(3)合成螯合剂或含染料的二苯并环辛炔(DIBO或DBCO)
(4)含叠氮化物的抗体和含染料的二苯并环辛炔通过点击化学进行偶联,最后5)使用放射性核素选择性地对位点修饰后抗体进行放射性标记(图6)。
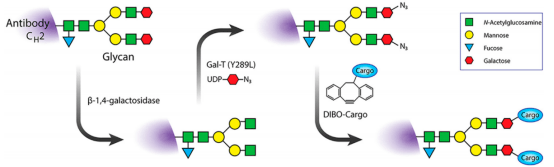
图6.一种可特异性将螯合剂等嫁接到抗体的重链聚糖上的化学酶方法示意图
该方法已应用于设计结直肠癌PET和光学成像的双标记药物。最近的一项研究表明使用这种化学酶策略开发的Zr-DFO-曲妥珠单抗较其通过随机偶联方法开发的对应物更优,由于其位点特异性的修饰,Zr-DFO-曲妥珠单抗在免疫PET成像研究中显示出增强的免疫反应性和稳定性。虽然能够得到均一且标准化的产品,但这种生产条件相对来说步骤冗长且苛刻。
3.3 一种突变的细菌卤烷脱卤酶
该系统的分子机制是基于一种从红球菌中获得的突变的细菌卤代烷烃脱卤酶。此技术通过使HaloTag(33 kDa)与目标蛋白质融合,然后引入一个Halotag的特异性配体,使其在Halotag修饰的蛋白质和配体之间形成一个不可逆的共价键(图7)。众所周知,His-tag在蛋白质生产中被广泛引入,但其作用仅限于蛋白质的分离和纯化。相比之下,HaloTag可以用于快速纯化蛋白质,并同分离出的蛋白质实现进一步的分子成像。已有初步证据证明了基于Halotag的预靶向成像的可行性。这种策略包括首先使用Halotag修饰的抗体进行预靶向,然后使用一个循环时间较短的小放射性标记分子进行成像。
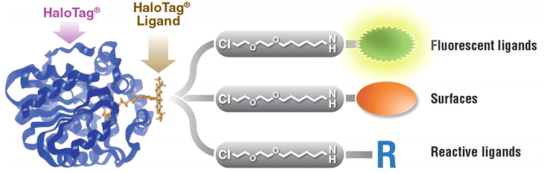
图7.HaloTag蛋白与特定的HaloTag配体形成共价键,每个HaloTag配体都包含一个结合基团和功能基团.
除上述介绍的几种酶外,微生物谷氨酰胺转移酶(mTGase)可通过化学计量学的方式修饰单克隆抗体,这种位点特异性工程的单克隆抗体对分子成像特别有意义;另一种细菌酶硫辛酸连接酶(LplA)也与氟辛酸([18F]FA)一起用于Fab片段的位点特异性放射性标记。虽然mTGase和LplA在介导生物分子的位点特异性放射性标记方面显示出了潜力,但它们的稳健性仍有待于未来的研究来证实。
4. Dock-and-Lock方法
为了进一步推进预靶向成像和治疗的临床转化和应用,一种更创新的方法(Dock-and-Lock)正在被用来大规模开发人源化重组Bsab。其中一个例子是Anti-CEA及Anti-HSG TF2 的BsAb,它包含一个来自Anti-HSG单抗679的人源化Fab片段和一个来自hMN14单抗(拉贝妥珠单抗)的两个人源化Anti-CEA的Fab片段。(图8)
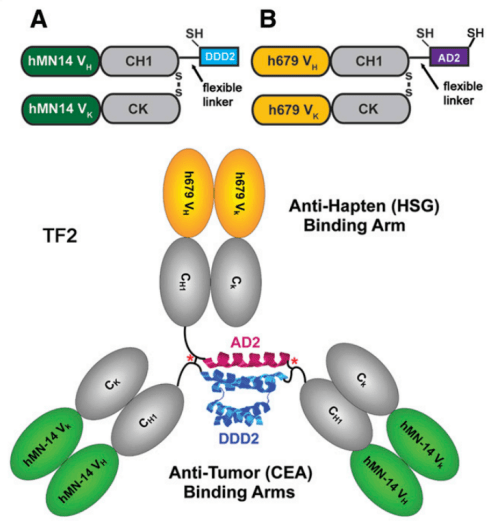
图8:anti-CEA × anti-HSG TF2 BsAb Dock-and-Lock示意图
作为预靶向系统中的半抗原肽,放射性标记的小分子具有两个HSG基团和各种螯合剂(图9),这种条件允许其使用不同感兴趣的放射性核素进行多功能标记。目前,已经通过这种方法产生了其他几种这样的Bsab。例如,CD20的TF4和粘蛋白抗原的TF10,也被积极的研究用于治疗目的。
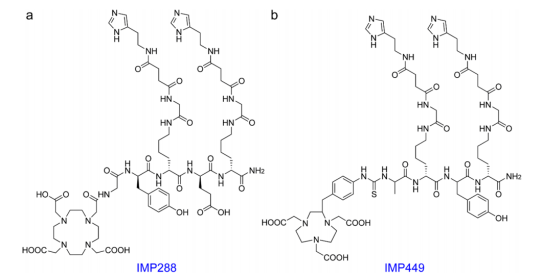
图9.DOTA-HSG和免疫PET成像中HSG半抗原肽的化学结构。
小 结
分子成像已成为癌症研究中的重要工具,既可以用于了解疾病的潜在生物学,也可以用于诊断和治疗。随着PET工程技术的不断发展,除了上述我们介绍到的几种放射性核素标记策略,越来越多的偶联方法将被开发。同时,选择合适的放射性核素标记策略(例如,放射性金属核素的标记策略不适合选择由Cu(I)催化的加成反应),可以帮助我们成功开发新的分子成像探针,也有助于在成像或是肿瘤杀灭中取得更好的效果。除了偶联策略,在免疫PET中每一步的选择对于杀灭肿瘤或是成像来说都是关键步骤。
本文转载自其他网站,不代表健康界观点和立场。如有内容和图片的著作权异议,请及时联系我们(邮箱:guikequan@hmkx.cn)
本文来自投稿,不代表长河网立场,转载请注明出处: http://www.changhe99.com/a/yBrgZP1g6P.html

