作者:生物谷
炎症过激活是脓毒症器官损伤发生的决定因素。心肌收缩和松弛是消耗能量的过程,高度依赖线粒体ATP供应。线粒体质量控制(mitochondrial quality control,MQC) 是一种细胞内源性保护程序,用于维持线粒体稳态。该系统调节线粒体分裂/融合,线粒体自噬和生物发生,以修复或去除结构不良的线粒体,从而维持线粒体功能和ATP的产生。增加融合或减少分裂可减少碎片线粒体的形成,同时线粒体自噬有助于消除无法修复的细胞器。尽管在脓毒性心肌病 (SCM) 中观察到线粒体损伤,但相关的MQC功能障碍和调节机制仍不清楚。
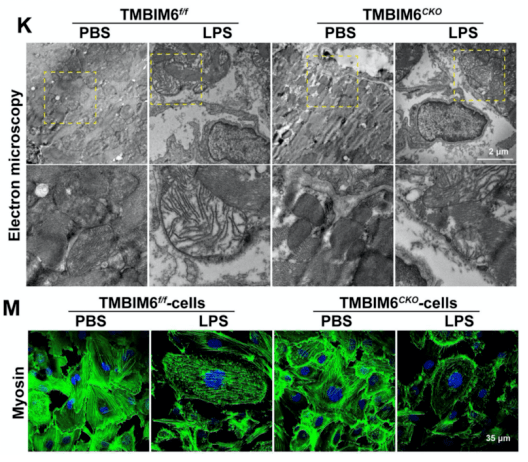
2023年1月,王艺瑾团队在Metabolism-Clinical and Experimental (中科院一区)发表题为TMBIM6 prevents VDAC1 multimerization and improves mitochondrial quality control to reduce sepsis-related myocardial injury的研究论文。作者构建了心肌细胞特异性TMBIM6敲除小鼠 (TMBIM6CKO) 和TMBIM6转基因小鼠 (TMBIM6TG),揭示了TMBIM6-VDAC1相互作用可以阻止VDAC1寡聚化,从而维持体内线粒体Ca2+平衡以及正常的MQC过程,有助于改善SCM的心肌功能。本研究揭示了TMBIM6在脓毒症中通过维持[Ca2+]m稳态,从而改善心肌细胞中的线粒体动态平衡,为进一步了解脓毒症相关线粒体功能障碍的分子机制提供了新的见解。预防脓毒症相关TMBIM6下调的策略可能有助于通过保留VDAC1单体构象状态来缓解脓毒症诱导的心肌损伤。
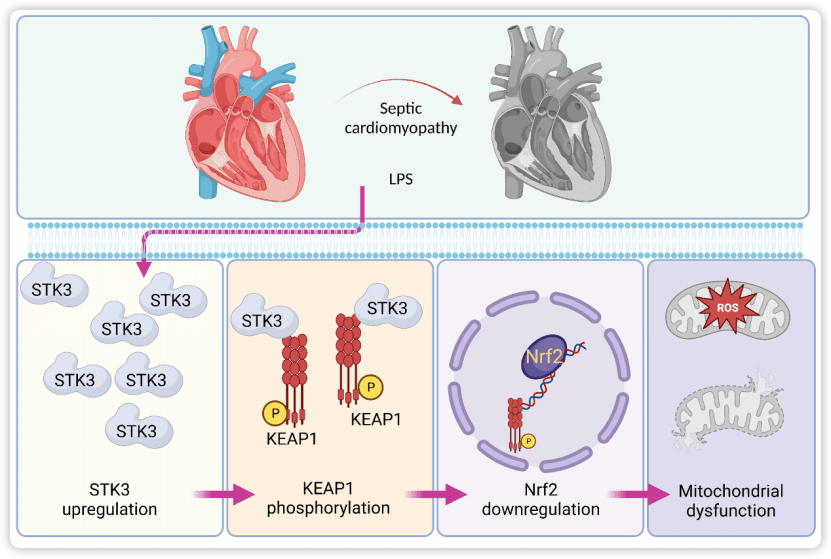
丝氨酸/苏氨酸激酶3(STK3),也被称为哺乳动物无菌20样激酶1(Mst1),是影响细胞凋亡和氧化应激的Hippo途径的核心成分。STK3的几个底物已被报道,包括GULT1、MAPK、NLRP3、LTB4、SAV1等。以前的研究结果主要阐明了STK3在多种心血管疾病下的病理作用,如糖尿病心肌病、儿茶酚胺诱发的心肌病、以及应激性心肌肥大。然而,STK3在脓毒症心肌病中的作用未见报道。
2023年3月,王艺瑾团队在Int J Biol Sci上发表题为Serine/threonine kinase 3 promotes oxidative stress and mitochondrial damage in septic cardiomyopathy through inducing Kelch-like ECH-associated protein 1 phosphorylation and nuclear factor erythroid 2-related factor 2 degradation的研究论文。作者构建了STK3敲除小鼠 (STK3-/-),揭示了STK3过度表达通过直接结合KEAP1并诱发其磷酸化,继而干扰KEAP1入核转位并由此下调Nrf2的转录,从而造成线粒体氧化应激损伤,最终扩大脓毒症条件下的心功能障碍。阻止STK3上调、逆转KEAP1磷酸化、增强Nrf2转录的手段和药物,可能是预防或治疗脓毒症心肌病的关键手段。
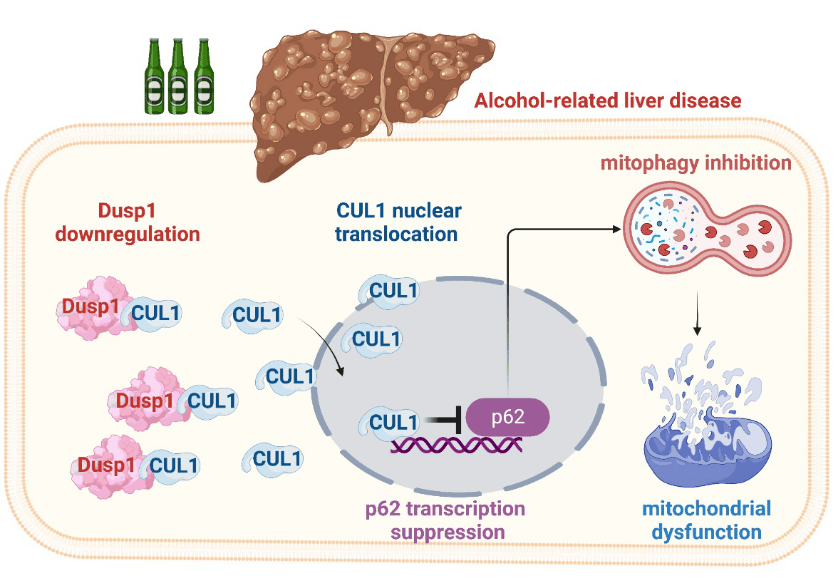
酒精性肝病(ALD)的特征是过量饮酒导致肝组织病变。ALD的唯一有效治疗方法是戒酒,但这对酒精性肝硬化患者的预后没有显著改善。探究酒精性肝损伤分子机制可为ALD的防治提供新的途径。
2023年3月,王艺瑾团队在Int J Biol Sci 上发表题为“Interaction between dual specificity phosphatase-1 and cullin-1 attenuates alcohol-related liver disease by restoring p62-mediated mitophagy”的研究论文。本文发现DUSP1下调是ALD发生的初始信号,DUSP1通过抑制线粒体自噬而导致线粒体功能障碍。在生理条件下,DUSP1与胞浆中的CUL1结合,阻止其易位到细胞核。酒精暴露后,DUSP1的表达减少,导致CUL1解离并穿梭到细胞核中,作为转录抑制物抑制Parkin和p62的表达。后者与线粒体自噬受损有关,并损害ATP的生成。通过DUSP1过表达或CUL1缺失来恢复线粒体自噬功能可以极大地减轻ALD肝细胞线粒体功能障碍。
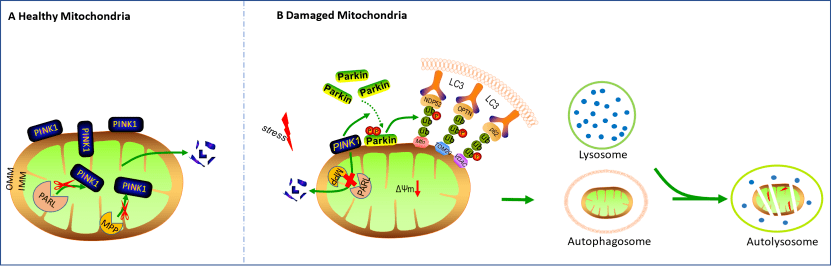
肝脏疾病是全球患者死亡的重要原因。线粒体功能障碍与多种急慢性肝病相关。线粒体自噬可以选择性地降解受损线粒体,维持线粒体网络功能的完整性和细胞稳态。在生理状态下,线粒体自噬起到保护肝脏免受组织损伤、维持肝脏稳态的作用。而线粒自噬受损或过激活在肝病发病机制中起重要作用。线粒体自噬介导的线粒体降解途径、线粒体自噬在肝脏疾病中的稳态失衡以及改变线粒体自噬是否可以作为肝脏病治疗靶点已有广泛研究。
2023年3月,王艺瑾团队在Antioxidants & Redox Signaling发表题为“The Role and Mechanism of Action of Mitophagy in Various Liver Diseases”的长篇综述,总结了线粒体自噬在各种肝脏疾病中的作用以及以线粒体自噬为靶点的潜在的治疗方案,对肝脏疾病发病机制及治疗具有重要意义。
通讯作者简介:

王艺瑾
南方科技大学医学院副教授,博士生导师
深圳市海外高层次人才
北京市科技新星计划获得者
欧洲肝病学会青年科学奖获得者
中国戊型肝炎研究协作组(CCSHE)组长
中国研究型医院学会肝病专委会青年委员会副主委
以第一/通讯作者在国际学术期刊Lancet RM, Science Advances, Gastroenterology, Hepatology, Journal of Hepatology, Medicine, EBioMedicine发表论文多篇,他引7000余次,入选2022全球前2%顶尖科学家榜单。
研究领域:
1、肝炎病毒-宿主互作、抗病毒天然免疫机制及策略
2、脓毒症发病机制
3、线粒体稳态在感染及谢性疾病中的调控机制
4、脂肪肝发病机制
5、肝脏肿瘤
本文转载自其他网站,不代表健康界观点和立场。如有内容和图片的著作权异议,请及时联系我们(邮箱:guikequan@hmkx.cn)
本文来自投稿,不代表长河网立场,转载请注明出处: http://changhe99.com/a/YQdZZYL8dD.html

